#cmsms_row_643626ab240a0 .cmsms_row_outer_parent {
padding-top: 0px;
}
#cmsms_row_643626ab240a0 .cmsms_row_outer_parent {
padding-bottom: 50px;
}
#cmsms_heading_643626ab24f6b {
text-align:center;
margin-top:0px;
margin-bottom:20px;
}
#cmsms_heading_643626ab24f6b .cmsms_heading {
text-align:center;
}
#cmsms_heading_643626ab24f6b .cmsms_heading, #cmsms_heading_643626ab24f6b .cmsms_heading a {
font-weight:normal;
font-style:normal;
color:#3b94d1;
}
#cmsms_heading_643626ab24f6b .cmsms_heading_divider {
}
Les autorités nationales de réglementation des médicaments en Europe ne protègent pas les intérêts des patients
#cmsms_row_643626ab250d8 .cmsms_row_outer_parent {
padding-top: 0px;
}
#cmsms_row_643626ab250d8 .cmsms_row_outer_parent {
padding-bottom: 50px;
}
#cmsms_row_643626ab2526f .cmsms_row_outer_parent {
padding-top: 0px;
}
#cmsms_row_643626ab2526f .cmsms_row_outer_parent {
padding-bottom: 50px;
}
Bristol (Royaume-Uni), Paris (France) et Amsterdam (Pays-Bas), 05 juillet 2021
Selon un nouveau rapport, les autorités nationales de réglementation des médicaments en Europe ne parviennent pas à garantir que les données sur les médicaments et les vaccins susceptibles de sauver des vies soient rapidement et systématiquement rendues publiques, comme l’exigent les règles de transparence établies de longue date par l’Union européenne.
Les régulateurs nationaux sont chargés de veiller à ce que les entreprises pharmaceutiques, les universités et les hôpitaux qui procèdent à des essais cliniques dans leur pays rendent les résultats des essais publics sur le registre européen des essais dans les 12 mois suivant la fin de l’essai.
Cependant, des milliers de résultats d’essais ne figurent actuellement pas dans le registre, ce qui ralentit le progrès médical et laisse des lacunes dans la base de preuves médicales qui nuisent aux patients, compromettent la santé publique et gaspillent les fonds publics destinés à la recherche. En outre, l’inaction des régulateurs nationaux a laissé le registre criblé de données inexactes et manquantes, ce qui empêche de déterminer de manière fiable quels traitements et vaccins sont actuellement testés dans le cadre d’essais et où en sont les essais individuels.
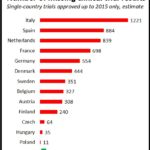
Le rapport et l’ensemble des données qui l’accompagnent montrent des différences significatives dans les performances des différents régulateurs. Parmi les plus grands régulateurs, ceux de France (ANSM), d’Italie (AIFA) et des Pays-Bas (CCMO) ont des performances particulièrement faibles.
Le rapport, qui repose sur des données compilées par des chercheurs de l’Université d’Oxford, est publié conjointement par quatre groupes à but non lucratif : Health Action International, Melanoma Patient Network Europe, Transparency International France et TranspariMED.
Nicholas DeVito, chercheur au EBM DataLab de l’Université d’Oxford, qui a compilé et analysé les données utilisées dans le rapport, a déclaré :
« Il s’agit de la première analyse complète de la localisation des problèmes de qualité des données dans le registre européen des essais cliniques. Le registre devrait être une ressource précieuse pour comprendre les essais cliniques à travers l’Europe, mais il arrive souvent que nous ne sachions pas si un essai a eu lieu, quand il s’est terminé, ou si des résultats sont disponibles pour cet essai. L’utilité du registre est gravement compromise par ces problèmes. »
Ellie White, responsable projets européens à Health Action International, a déclaré :
« Ce nouveau rapport opportun indique une sous-déclaration systémique des données des essais cliniques par les régulateurs de médicaments à travers l’Europe, mais il est important de se rappeler que la transparence n’est pas un but en soi. Sans une adhésion adéquate aux règles de transparence existantes de l’Union européenne, par le biais d’une mise en œuvre nationale, et sans que les informations soient systématiquement rendues publiques de manière compréhensible, nous ne pouvons pas espérer que les chercheurs et les institutions publiques utilisent les données disponibles et évitent ainsi le risque de gaspillage de la recherche et d’autres dysfonctionnements. Ce rapport présente des recommandations politiques simples et réalisables dont nous espérons que les régulateurs nationaux et les autres parties prenantes tiendront compte. »
Le Dr Till Bruckner, fondateur de TranspariMED, a déclaré :
« De nombreux régulateurs nationaux à travers l’Europe ne contactent même pas les entreprises pharmaceutiques et les universités qui enfreignent les règles, et encore moins, ne les sanctionnent. La négligence des régulateurs a entraîné de longs retards dans la publication des résultats des essais cliniques et un gaspillage coûteux de la recherche. Les patients qui attendent désespérément de nouveaux et meilleurs traitements contre le Covid, le cancer et d’autres maladies potentiellement mortelles méritent mieux. Les régulateurs doivent cesser de fermer les yeux et prendre immédiatement des mesures pour s’assurer que tous les résultats d’essais cliniques manquants soient rendus publics aussi rapidement que possible, d’autant plus que de nombreux essais de médicaments Covid doivent rendre leurs résultats plus tard dans l’année. »
Patrick Lefas, président de Transparency International France, partenaire du rapport, a déclaré :
« Transparency International France souhaite que dans l’intérêt de la recherche médicale et du bien-être des patients, l’ANSM adopte, comme elle s’y est engagée, une attitude plus active vis-à-vis des promoteurs d’essais cliniques publics et privés afin de les inciter à se mettre en conformité avec leurs obligations de transparence. Sans quoi les obligations légales européennes, même les plus ambitieuses, resteront des déclarations d’intention. »
Deux autres groupes qui ont examiné une copie préliminaire du rapport ont également exhorté les régulateurs à prendre des mesures.
Natalie Rhodes, responsable des politiques de Transparency International Global Health, a déclaré :
« Bien qu’elle s’inscrive dans le même paysage politique, cette étude met en évidence le niveau extrêmement variable, et inquiétant, de conformité aux normes de transparence des essais cliniques entre les pays européens. Ce rapport dresse un tableau sombre et souligne la nécessité de prendre la transparence beaucoup plus au sérieux par les chercheurs, les promoteurs d’essais cliniques et les organismes de réglementation en Europe. Si de nombreux progrès ont été accomplis dans ce domaine, il est clair qu’il reste encore beaucoup à faire. »
Le Dr Karla Soares-Weiser, rédactrice en chef de la Cochrane Library, a déclaré :
« Cochrane est un fervent partisan des efforts visant à garantir la disponibilité des données de tous les essais cliniques. Pour évaluer l’efficacité et la sécurité d’une intervention en matière de soins de santé, nous devons savoir quelles études ont été réalisées, comment elles ont été menées et ce qu’elles ont révélé. Il est inquiétant de constater, à la lumière de cette nouvelle analyse, que plusieurs des agences nationales des médicaments en Europe ne remplissent pas pleinement leur devoir de veiller à ce que ces informations soient accessibles au public. Nous leur demandons instamment de prendre des mesures pour remédier à cette situation dans les plus brefs délais. »
Click here to change this text
#cmsms_heading_643626ab2a92b {
text-align:left;
margin-top:0px;
margin-bottom:20px;
}
#cmsms_heading_643626ab2a92b .cmsms_heading {
text-align:left;
}
#cmsms_heading_643626ab2a92b .cmsms_heading, #cmsms_heading_643626ab2a92b .cmsms_heading a {
font-weight:normal;
font-style:normal;
color:#3b94d1;
}
#cmsms_heading_643626ab2a92b .cmsms_heading_divider {
}
EN SAVOIR PLUS
#cmsms_button_643626ab2b503 {
text-align:center;
}
#cmsms_button_643626ab2b503 .cmsms_button:before {
margin-right:.5em;
margin-left:0;
vertical-align:baseline;
}
#cmsms_button_643626ab2b503 .cmsms_button {
font-weight:normal;
font-style:normal;
border-style:solid;
background-color:#3b94d1;
}
#cmsms_button_643626ab2b503 .cmsms_button:hover {
}
#cmsms_divider_643626ab2c287 {
border-bottom-width:1px;
border-bottom-style:solid;
padding-top:50px;
margin-bottom:50px;
}
#cmsms_button_643626ab2d217 {
text-align:center;
}
#cmsms_button_643626ab2d217 .cmsms_button:before {
margin-right:.5em;
margin-left:0;
vertical-align:baseline;
}
#cmsms_button_643626ab2d217 .cmsms_button {
font-weight:normal;
font-style:normal;
border-style:solid;
background-color:#3b94d1;
}
#cmsms_button_643626ab2d217 .cmsms_button:hover {
}
#cmsms_divider_643626ab2deea {
border-bottom-width:1px;
border-bottom-style:solid;
padding-top:50px;
margin-bottom:50px;
}
#cmsms_row_643626ab2e1e9 .cmsms_row_outer_parent {
padding-top: 0px;
}
#cmsms_row_643626ab2e1e9 .cmsms_row_outer_parent {
padding-bottom: 50px;
}